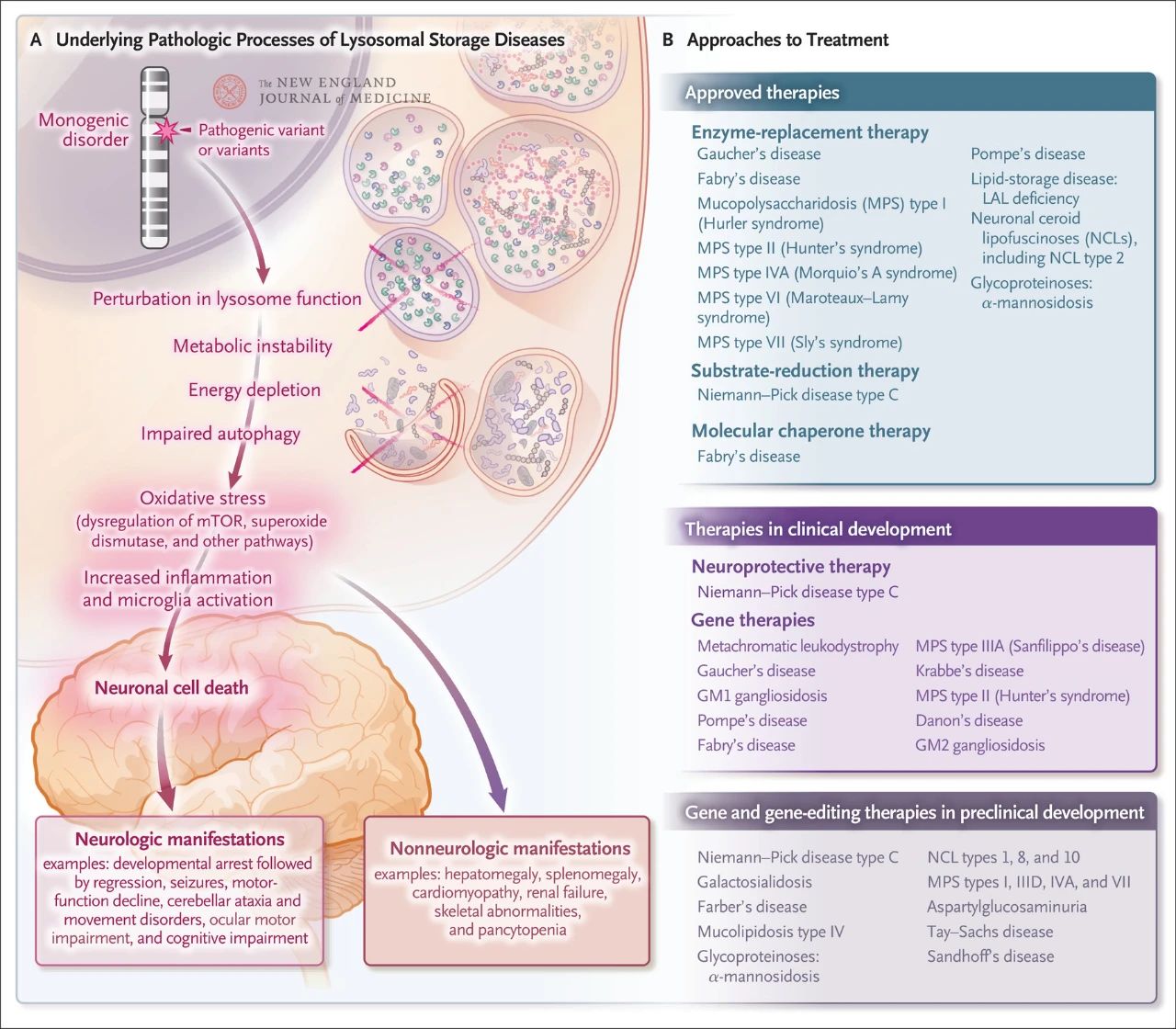
Deși relativ rară, incidența generală a depozitării lizozomale este de aproximativ 1 la fiecare 5.000 de nașteri vii. În plus, din cele aproape 70 de tulburări de depozitare lizozomale cunoscute, 70% afectează sistemul nervos central. Aceste tulburări monogenice provoacă disfuncții lizozomale, rezultând instabilitate metabolică, disreglare a proteinei țintă a rapamicinei la mamifere (mTOR, care în mod normal inhibă inflamația), afectare a autofagiei și moartea celulelor nervoase. Au fost aprobate sau sunt în curs de dezvoltare mai multe terapii care vizează mecanismele patologice care stau la baza bolii de depozitare lizozomale, inclusiv terapia de substituție enzimatică, terapia de reducere a substratului, terapia cu chaperone moleculare, terapia genică, editarea genelor și terapia neuroprotectoare.
Boala Niemann-Pick de tip C este o tulburare de transport celular al colesterolului cu stocare lizozomală cauzată de mutații bialelice fie în NPC1 (95%), fie în NPC2 (5%). Simptomele tipului C al bolii Niemann-Pick includ declin neurologic rapid și fatal în copilărie, în timp ce formele juvenile tardive, juvenile și cu debut la vârsta adultă includ splenomegalie, paralizie supranucleară a privirii și ataxie cerebeloasă, dizarticulație și demență progresivă.
În această ediție a revistei, Bremova-Ertl și colab. prezintă rezultatele unui studiu clinic crossover, dublu-orb, controlat cu placebo. Studiul a utilizat un potențial agent neuroprotector, analogul de aminoacid N-acetil-L-leucină (NALL), pentru a trata boala Niemann-Pick de tip C. Aceștia au recrutat 60 de pacienți adolescenți și adulți simptomatici, iar rezultatele au arătat o îmbunătățire semnificativă a scorului total (criteriu final principal) al Scalei de Evaluare și Rating a Ataxiei.
Studiile clinice ale N-acetil-DL-leucinei (Tanganil), un racemic al NALL și n-acetil-D-leucinei, par a fi determinate în mare măsură de experiență: mecanismul de acțiune nu a fost clar elucidat. N-acetil-dl-leucina a fost aprobată pentru tratamentul vertijului acut încă din anii 1950; Modelele animale sugerează că medicamentul funcționează prin reechilibrarea suprapolarizării și depolarizării neuronilor vestibulari mediali. Ulterior, Strupp și colab. au raportat rezultatele unui studiu pe termen scurt în care au observat îmbunătățiri ale simptomelor la 13 pacienți cu ataxie cerebeloasă degenerativă de diverse etiologii, constatări care au reaprins interesul pentru reexaminarea medicamentului.
Mecanismul prin care n-acetil-DL-leucina îmbunătățește funcția nervoasă nu este încă clar, dar descoperirile la două modele murine, unul cu boala Niemann-Pick de tip C și celălalt cu tulburarea de depozitare a gangliozidelor GM2 varianta O (boala Sandhoff), o altă boală lizozomală neurodegenerativă, au determinat atenția asupra NALL. Mai exact, supraviețuirea șoarecilor Npc1-/- tratați cu n-acetil-DL-leucină sau NALL (enantiomeri L) s-a îmbunătățit, în timp ce supraviețuirea șoarecilor tratați cu n-acetil-D-leucină (enantiomeri D) nu s-a îmbunătățit, sugerând că NALL este forma activă a medicamentului. Într-un studiu similar privind tulburarea de depozitare a gangliozidelor GM2 varianta O (Hexb-/-), n-acetil-DL-leucina a dus la o prelungire modestă, dar semnificativă, a duratei de viață la șoareci.
Pentru a explora mecanismul de acțiune al n-acetil-DL-leucinei, cercetătorii au investigat calea metabolică a leucinei prin măsurarea metaboliților din țesuturile cerebeloase ale animalelor mutante. Într-o variantă O a modelului tulburării de stocare a gangliozidelor GM2, n-acetil-DL-leucina normalizează metabolismul glucozei și glutamatului, crește autofagia și crește nivelurile de superoxid dismutază (un agent activ de eliminare a oxigenului). În modelul C al bolii Niemann-Pick, s-au observat modificări ale metabolismului glucozei și antioxidantului și îmbunătățiri ale metabolismului energetic mitocondrial. Deși L-leucina este un activator puternic al mTOR, nu a existat nicio modificare a nivelului sau fosforilării mTOR după tratamentul cu n-acetil-DL-leucină sau enantiomerii săi la niciunul dintre modelele de șoarece.
Efectul neuroprotector al NALL a fost observat într-un model murin de leziuni cerebrale induse de impact cortical. Aceste efecte includ scăderea markerilor neuroinflamatori, reducerea morții celulelor corticale și îmbunătățirea fluxului autofagic. După tratamentul cu NALL, funcțiile motorii și cognitive ale șoarecilor răniți au fost restabilite, iar dimensiunea leziunii a fost redusă.
Răspunsul inflamator al sistemului nervos central este caracteristica majorității tulburărilor neurodegenerative de depozitare lizozomală. Dacă neuroinflamația poate fi redusă prin tratamentul cu NALL, simptomele clinice ale multor, dacă nu ale tuturor, tulburărilor neurodegenerative de depozitare lizozomală ar putea fi ameliorate. După cum arată acest studiu, se așteaptă ca NALL să aibă sinergii și cu alte terapii pentru boala de depozitare lizozomală.
Multe tulburări de depozitare lizozomală sunt, de asemenea, asociate cu ataxia cerebeloasă. Conform unui studiu internațional care a implicat copii și adulți cu tulburări de depozitare a gangliozidelor GM2 (boala Tay-Sachs și boala Sandhoff), ataxia a fost redusă și coordonarea motorie fină s-a îmbunătățit după tratamentul cu NALL. Cu toate acestea, un studiu amplu, multicentric, dublu-orb, randomizat, controlat cu placebo, a arătat că n-acetil-DL-leucina nu a fost eficientă clinic la pacienții cu ataxie cerebeloasă mixtă (ereditară, neereditară și inexplicabilă). Această constatare sugerează că eficacitatea poate fi observată numai în studiile care au implicat pacienți cu ataxie cerebeloasă ereditară și mecanismele de acțiune asociate analizate. În plus, deoarece NALL reduce neuroinflamația, care poate duce la leziuni cerebrale traumatice, pot fi luate în considerare studiile privind NALL pentru tratamentul leziunilor cerebrale traumatice.
Data publicării: 02 martie 2024